A Anvisa Fiscaliza Medicamentos Emagrecedores e implementa um conjunto de novas regulamentações para intensificar o controle sanitário sobre fármacos injetáveis voltados para a perda de peso. A medida, anunciada na segunda-feira, 6 de abril de 2026, abrange especificamente os agonistas de GLP-1, que incluem substâncias amplamente utilizadas como semaglutida, tirzepatida e liraglutida.
Esta decisão regulatória surge em resposta a um aumento significativo de irregularidades identificadas tanto na importação de insumos farmacêuticos quanto na produção por parte de farmácias de manipulação em todo o território nacional. As ações planejadas pela agência incluem a revisão das normas vigentes, uma intensificação notável nas fiscalizações e a potencial suspensão das atividades de estabelecimentos que apresentem riscos sanitários. Além disso, a Anvisa (Agência Nacional de Vigilância Sanitária) planeja expandir as inspeções em empresas responsáveis pela importação de insumos farmacêuticos e fortalecer parcerias com agências reguladoras internacionais para um controle mais robusto. A criação de um grupo de trabalho multidisciplinar, envolvendo entidades médicas e representantes do setor de saúde, também está prevista para acompanhar de perto a evolução do tema e garantir a segurança dos pacientes.
Anvisa Fiscaliza Medicamentos Emagrecedores e Irregularidades
De acordo com a agência, o objetivo primordial dessas iniciativas é conter práticas que podem colocar em risco a saúde e a segurança dos pacientes. O diretor Leandro Safatle enfatizou que as novas diretrizes não visam proibir a manipulação de medicamentos, mas sim aprimorar o arcabouço normativo existente para assegurar a qualidade e a segurança dos produtos. “Não estamos proibindo a manipulação. O que está sendo feito é o aperfeiçoamento desse normativo para possibilitar e dar essa garantia”, afirmou Safatle, destacando o compromisso da Anvisa com a saúde pública.
Dados compilados pela própria Anvisa revelam uma notável discrepância entre o volume de insumos farmacêuticos importados e a demanda projetada para o país. No segundo semestre de 2025, por exemplo, o Brasil recebeu aproximadamente 130 quilos dessas substâncias, uma quantidade suficiente para a produção de até 25 milhões de doses. Essa disparidade levanta preocupações sobre a destinação e o uso desses materiais.
Em um caso específico envolvendo a tirzepatida, os pedidos de importação registrados entre novembro de 2025 e abril de 2026 superaram a marca de 100 quilos, montante que corresponderia a cerca de 20 milhões de doses. Uma parcela significativa desses pedidos foi barrada; precisamente 14 solicitações foram negadas em março de 2026 devido a problemas relacionados ao controle de qualidade, evidenciando falhas nas etapas iniciais da cadeia de suprimentos.
A fiscalização da Anvisa também identificou falhas cruciais na cadeia de produção e distribuição. Em 2026, a agência realizou 11 inspeções, superando o número total de fiscalizações do ano anterior. Essas inspeções resultaram na interdição de oito empresas, que incluíam tanto farmácias de manipulação quanto uma importadora. Os problemas mais recorrentes identificados foram falhas nos processos de esterilização, a ausência de um controle de qualidade adequado e o uso de insumos sem a devida comprovação de origem. No total, mais de 1,3 milhão de unidades de produtos estéreis foram apreendidas em decorrência dessas ações fiscalizatórias.
Outro ponto de grande preocupação é o crescente número de relatos de efeitos adversos associados ao uso desses medicamentos. O sistema VigiMed da Anvisa tem registrado um aumento nas notificações, muitas das quais não incluem uma identificação clara da origem do produto. Um estudo citado pela agência aponta que aproximadamente 26% dos casos de efeitos adversos estão ligados ao uso desses medicamentos fora das indicações aprovadas em bula, prática conhecida como uso off-label, o que eleva consideravelmente os riscos à saúde dos pacientes.
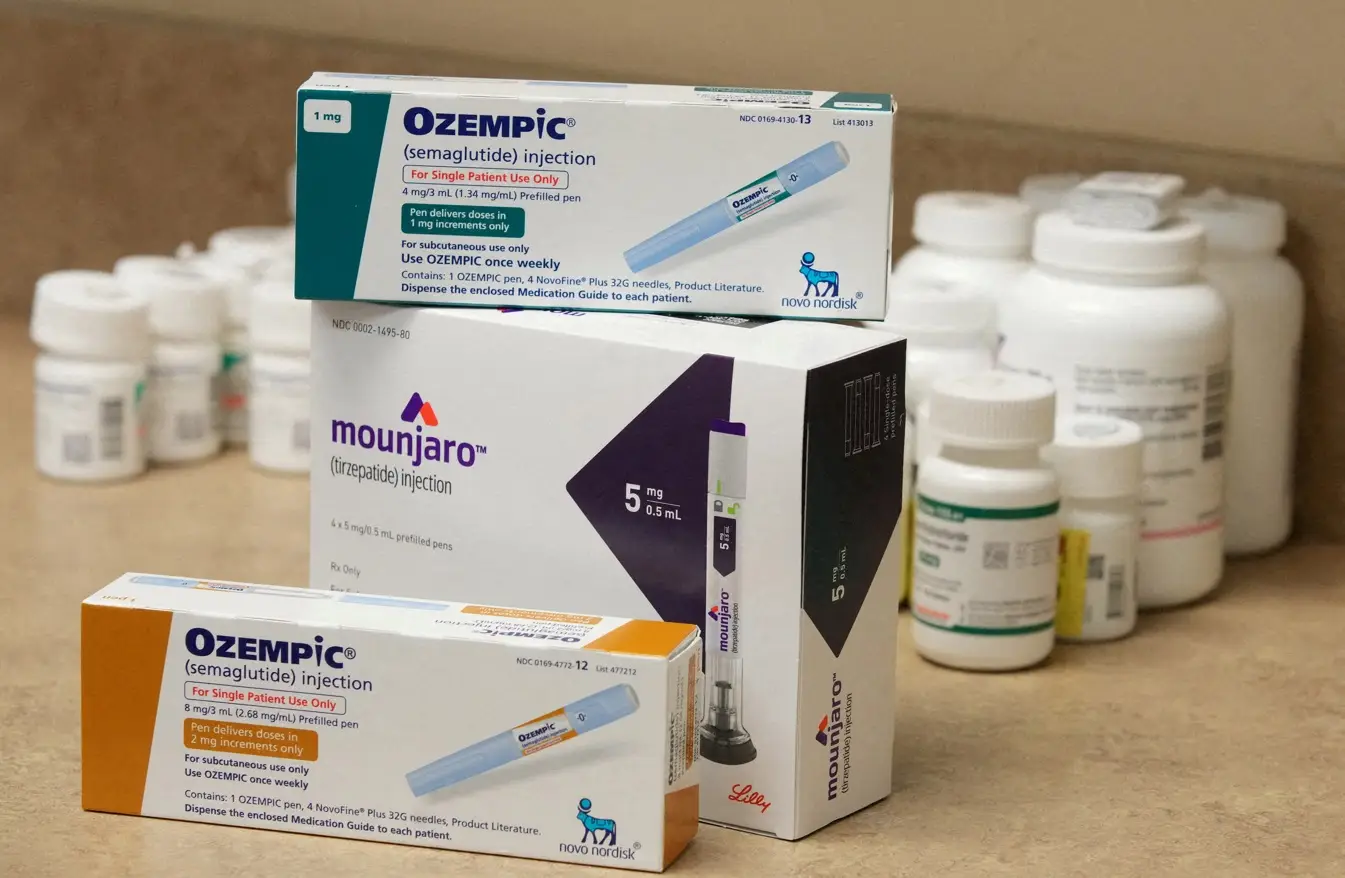
Imagem: REUTERS via infomoney.com.br
O interesse por medicamentos que contêm semaglutida, substância popularizada tanto para o tratamento de diabetes quanto para o emagrecimento, está projetado para crescer ainda mais. Este cenário é impulsionado pela expiração da patente da semaglutida no Brasil em março de 2026, o que abre caminho para a entrada de novos produtos no mercado farmacêutico. Atualmente, a Anvisa possui oito pedidos em processo de análise para medicamentos com este princípio ativo, e outros nove aguardam o início da avaliação técnica. Contudo, a agência reitera que nenhum produto pode ser comercializado sem a devida comprovação de eficácia, segurança e qualidade, atributos que devem ser atestados por meio de um registro oficial junto ao órgão regulador. Para informações adicionais sobre as regulamentações sanitárias, consulte o portal oficial da Anvisa.
A Anvisa avalia que o reforço regulatório implementado é fundamental para acompanhar a expansão contínua desse mercado e garantir que o aumento da oferta de medicamentos ocorra sempre em conformidade com os rigorosos padrões sanitários exigidos, protegendo assim a saúde da população brasileira.
Confira também: Imoveis em Rio das Ostras
Em resumo, as novas medidas da Anvisa representam um passo crucial para assegurar a segurança e a eficácia dos medicamentos injetáveis para emagrecimento no Brasil, combatendo irregularidades e protegendo os consumidores. Para se manter atualizado sobre as últimas notícias e análises no setor de saúde e regulamentação, continue acompanhando nossa editoria de Análises.
Crédito da imagem: Agência Brasil


